Исследование AVENANCE: Беспрецедентная ОВ 40,8 месяцев в уротелиальном раке при применении режима JAVELIN Bladder 100 в 1 линии

На конгрессе ASCO GU 2024 были представлены результаты рутинной клинической практики применения режима JavelinBladder 100* у более 1 200 пациентов в исследованиях AVENANCE (Франция), PATRIOT-II (США) и READY CUP (Италия).
Ключевые выводы:
- Несмотря на включение более ослабленных пациентов, реальная клиническая практика подтверждает эффективность и благоприятный профиль безопасности поддерживающей терапии Бавенсио® (авелумаб), продемонстрированные в исследовании Javelin Bladder 100.
- Согласно результатам поданализа AVENANCE, у пациентов, получавших терапию конъюгатом моноклонального антитела с лекарственным средством (ADC) после режима JAVELIN Bladder, медиана ОВ с начала химиотерапии первой линии достигла 40,8 месяцев в условиях рутинной клинической практики.

- Исследования рутинной клинической практики в Италии и США показали, что медиана общей выживаемости от начала химиотерапии первой линии составила около 30 месяцев для пациентов, получавших поддерживающую терапию при отсутствии прогрессии заболевания по окончании химиотерапии препаратами платины в 1 линии, что подтверждает результаты регистрационного клинического исследования.
Подробнее об AVENANCE
Последовательность терапии при УР определяет эффективность лечения:
Согласно результатам крупнейшего исследования по эффективности поддерживающей терапии авелумабом в рутинной клинической практике во Франции AVENANCE (n=595), у пациентов без прогрессирования после химиотерапии первой линии медиана общей выживаемости составляет 26,5 месяцев от начала терапии 1Л.
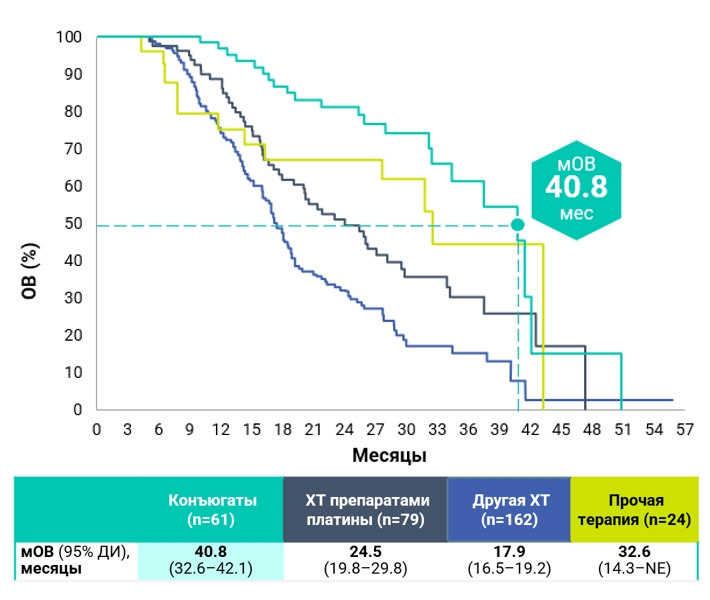
Более 70% пациентов, окончивших терапию БАВЕНСИО®, получали 2Л терапии
В рамках подгруппового анализа оценивались результаты 330 пациентов, получавших терапию второй линии. У 62 пациентов, получавших ADC-терапию (энфортумаб ведотин: n=56; сацитузумаб говетикан: n=6), мОВ от начала 1Л терапии составила 40,8 месяцев (95% ДИ, 32,6 – 42,1). У 81 пациента, пролеченных во 2Л ХТ препаратами платины, мОВ – 24,5 месяца (95% ДИ, 19,8 – 29,8). После ≥2 лет наблюдения большинство пациентов остается на терапии: 21% продолжает поддерживающую терапию Бавенсио® и 55,5% получают 2 линию терапии.

Подробнее о READY-CUP и PATRIOT-II
Долгосрочная эффективность режима JAVELIN Bladder в реальной клинической практике
- Исследование в реальной клинической практике READY CUP, Италия (n=464):
Проспективная неинтервенционная программа расширенного доступа (CUP) обеспечила пациентам в Италии с м/р или мУР возможность получения поддерживающей терапии первой линии препаратом БАВЕНСИО®. При медиане наблюдения 20,3 месяца (95% ДИ, 19,8 – 20,9), медиана ОВ от начала химиотерапии первой линии составила 30,9 месяцев (95% ДИ, 25,7 – НД) у пациентов без прогрессирования после химиотерапии 1Л. Медиана ОВ от начала поддерживающей терапии составила 26.2 месяца (95% ДИ, 20,0 – НД). - Исследование в реальной клинической практике PATRIOT-II, США (n=160):
В рамках наблюдательного ретроспективного исследования PATRIOT-II были проанализированы истории болезни 160 американских пациентов с медианой наблюдения с начала поддерживающей терапии препаратом БАВЕНСИО® 16 месяцев (диапазон 11-21 месяцев). Пациенты, получившие поддерживающую терапию первой линии препаратом БАВЕНСИО®, после химиотерапии достигали медианы ОВ 30,5 месяца от начала 1 линии терапии (95% ДИ, 23,4 – 37,6), медиана ОВ от начала поддерживающей терапии составила 24,4 месяца (95% ДИ, 20,4 – 28,4).
Дополнительные анализы данных
Анализ качества жизни и эффективности у пациентов с высоким ИМТ по данным Javelin Bladder 100
- Оценка переносимости пациентами:
В рамках ретроспективного анализа оценивались данные долгосрочных результатов, сообщаемых пациентами (PRO), с использованием Национальной комплексной онкологической сети/функциональной оценки индекса симптомов рака мочевого пузыря-18 (FBlSI-18) и EuroQoL «5 измерений 5 уровней». Оценки пациентов проводились по всем циклам до окончания лечения препаратом БАВЕНСИО®: изменение среднего значения от исходного уровня -2.15 (95% ДИ, -3,25 – -1,04) по FBISI-18 и -0,07 (95% ДИ, -0,09 – -0,05) по EQ-5D-5L. У пациентов с продолжительностью терапии препаратом БАВЕНСИО® 12 месяцев и более изменение среднего значения от исходного уровня составило 1,28 (95% ДИ, 0,08 – 2,49) по FBISI-18 и -0,02 по EQ-5D-5L, что свидетельствует об эффективности и хорошей переносимости режима JavelinBladder у пациентов с распространенным УР до прогрессирования или непереносимой токсичности. - Анализ подгруппы пациентов с высоким ИМТ:
Анализ подгруппы пациентов с высоким индексом массы тела (ИМТ; ≥30 кг/м2, n=122) показал эффективность и безопасность поддерживающей терапии препаратом БАВЕНСИО® у данной категории больных. Это ключевая популяция пациентов с учетом того, что высокий ИМТ – это фактор риска развития рака мочевого пузыря, а также увеличения населения с высоким ИМТ. У пациентов с высоким ИМТ (исходный уровень), получавших поддерживающую терапию препаратом БАВЕНСИО®, медиана ОВ составила 20,8 месяцев от начала поддерживающей терапии (95% ДИ, 16,9 – 34,4) по сравнению с 12,7 месяцами (95% ДИ, 8,1 – 26,6 месяцев) в группе наблюдения (ОР: 0,77; 95% ДИ, 0,49 – 1,21). Долгосрочная безопасность пациентов с высоким ИМТ соответствовала результатам лечения в общей когорте больных.

«Исследование JAVELIN Bladder 100 помогло решительно изменить стандарты лечения пациентов с распространенным уротелиальным раком после десятилетнего отсутствия значительных успехов. Продолжая предоставлять информацию о новых исследованиях препарата БАВЕНСИО®, включая данные о качестве жизни пациентов, ключевых популяциях пациентов и планировании последующей терапии, мы можем оказывать дальнейшую поддержку врачам при принятии информированных решений о лечении каждого отдельного пациента».
RU-AVE-00542| Февраль 2024 г.
*Режим Javelin Bladder 100 – платиносодержащая химиотерапия и последующая поддерживающая терапия препаратом Бавенсио® (авелумаб) в отсутствие прогрессирования на фоне химиотерапии в 1 линии.
Список литературы:
- Abstract No. 537. Presented at the ASCO Genitourinary Cancers Symposium, January 25-27, 2024; San Francisco, CA.
- Abstract No. 558. Presented at the ASCO Genitourinary Cancers Symposium, January 25-27, 2024; San Francisco, CA.
- Abstract No. 561. Presented at the ASCO Genitourinary Cancers Symposium, January 25-27, 2024; San Francisco, CA.
- Abstract No. 633. Presented at the ASCO Genitourinary Cancers Symposium, January 25-27, 2024; San Francisco, CA.
- Abstract No. 697. Presented at the ASCO Genitourinary Cancers Symposium, January 25-27, 2024; San Francisco, CA.
Инструкция по медицинскому применению препарата Бавенсио® (авелумаб). РУ: ЛП-005886
Материал предназначен для медицинских (фармацевтических) работников. © ООО «Мерк»: 115054, Москва, ул. Валовая, д. 35. Тел. +7 (495) 937-33-05. Веб-сайт: www.merckgroup.com/ru-ru Почта: russia@merckgroup.com Официальный сайт Мерк «Онкология в России»: https://merck.oncology.ru/
06.03.2024


